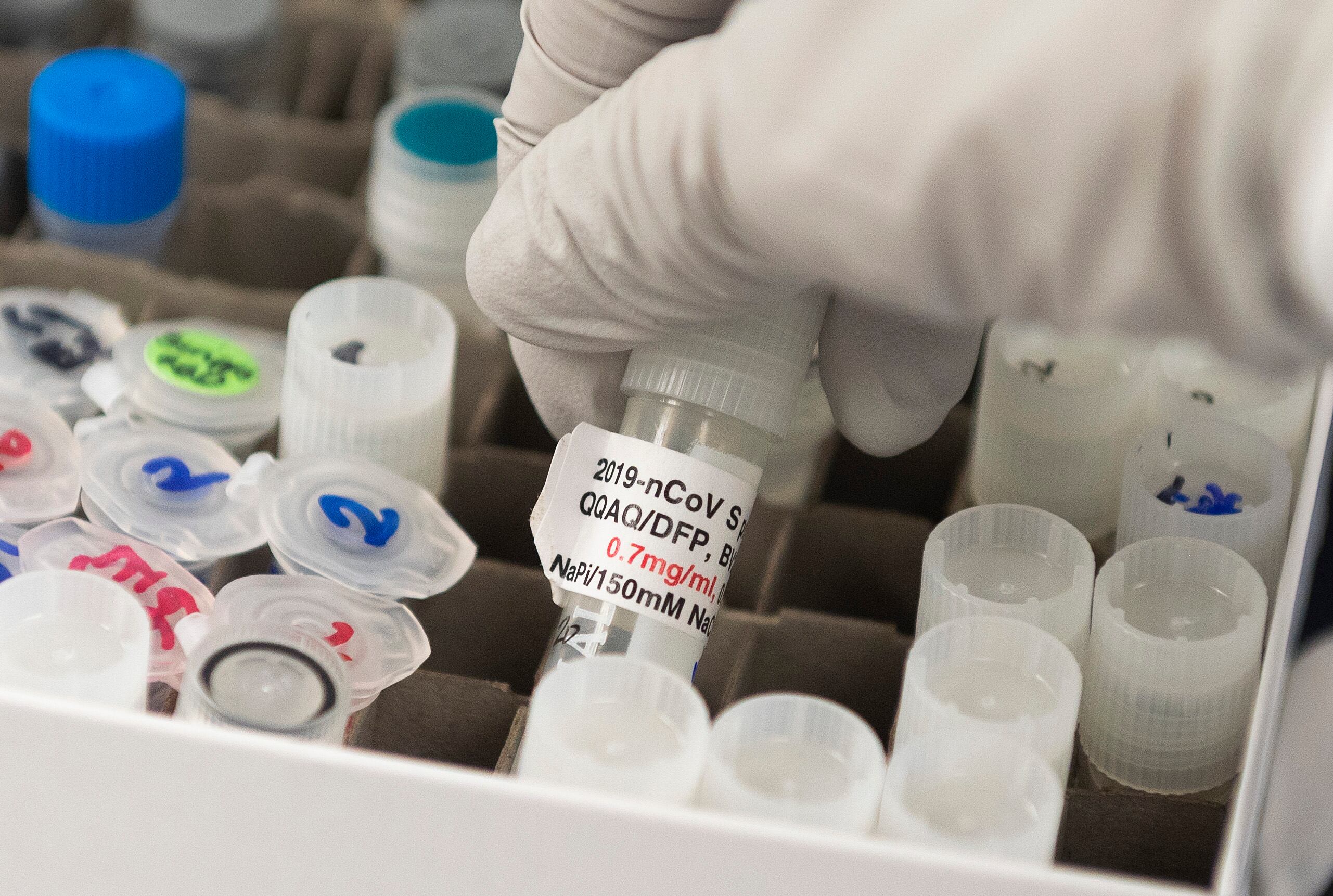
La compañía farmacéutica AstraZeneca anunció la tarde de este martes que pone en pausa su ensayo clínico para probar una vacuna contra la covid-19. La razón: un evento adverso grave en uno de sus participantes en el Reino Unido.
La noticia fue dada a conocer por el medio estadounidense STAT News.
No se detalló en qué consistió el efecto secundario y cuán raro es. No obstante, usualmente los que son denominados como efectos graves incluyen síntomas que requieren hospitalización, provocan enfermedades crónicas o discapacidades o incluso ponen en riesgo la vida de la persona.
Esto, sin embargo, no quiere decir que del todo se haya suspendido. Suspender un estudio mientras se evalúa no significa cancelar el ensayo ni que la vacuna no funcione o sea segura; lo que hace es interrumpir el reclutamiento de nuevos participantes y no aplicar dosis a quienes ya estaban reclutados pero aún no la habían recibido. Esto se mantendrá hasta que la situación se aclare.
Esto se hace para priorizar la seguridad de las personas.
El estudio estaba en la fase III de pruebas. La fase III es la última que se da antes de la aprobación, distribución y aplicación de un producto farmacéutico. Esta consiste en probar la vacuna experimental en una cantidad grande de personas (en este caso, eran más de 30.000 solo en EE. UU.).
El hecho de probarla en tantas personas verificará dos cosas: si la eficacia es la necesaria y si hay efectos adversos raros que se habían escapado en las dos primeras fases de estudios, y que los llama a revisar el producto para evitar estas situaciones.
“Entre más es la cantidad de personas que reciben un producto, mayores son las posibilidades de encontrar efectos raros o muy poco comunes”, explicó el farmacéutico Rigoberto López.
FUENTE: OMS || DISEÑO / LA NACIÓN.
Esto fue precisamente lo que sucedió con esta candidata a vacuna: al probarse en un número mayor de personas se dejó ver un efecto raro.
“El proceso de revisión estándar hizo que se diera una pausa en las pruebas para revisar los datos de seguridad”, dijo un vocero de la compañía farmacéutica a la periodista Helen Branswell, de STAT News.
El vocero añade: “es una acción de rutina que debe hacerse cuando se da un efecto inexplicable en uno de los ensayos clínicos. Se pone en pausa mientras se investiga. (...) La compañía trabaja en una revisión expedita de este evento para minimizar el impacto en la línea de tiempo del ensayo”.
Hasta el momento este es el primer ensayo en fase III para una vacuna contra la covid-19 que es puesto en pausa, pero esta situación no es inusual cuando se prueban productos médicos.
En julio pasado, la empresa publicó los resultados de las primeras fases del ensayo, el cual fue desarrollado junto con la Universidad de Oxford. El texto fue publicado en la revista The Lancet. Esta fase se realizó en 1.077 personas y se determinó que los efectos secundarios en las personas habían sido leves y moderados, y que estos incluían fiebre, dolor de cabeza, dolor y alergia en el sitio de la inyección y dolor muscular.
LEA MÁS: (Video) En 24 horas hubo 21 muertes asociadas al covid-19 en el país
¿Cómo es esta vacuna?
De todos los esfuerzos para encontrar una vacuna, esta en específico era uno de los que más adelantados se encontraba. En este momento hay 34 posibles vacunas a prueba en seres humanos, pero solo nueve en fase III de ensayos.
Esta vacuna experimental utiliza un virus genéticamente modificado para evitar que produzca infecciones.
Lo que se busca es vulnerar la llamada proteína S o spike del virus (la que le da la forma de corona y que es empleada como puerta de entrada a las células humanas). Además, se potencia el sistema inmunitario para reconocer al virus y hacerle frente si tuviera que exponerse a este.
Esta plataforma de virus genéticamente modificado no está presente en otras vacunas que ya se utilizan, pero sí se ha probado en otras, como la usada contra el ébola.
LEA MÁS: Costa Rica contacta tres farmacéuticas y prepara presupuesto para acceder a posible vacuna
Las otras opciones a prueba
De acuerdo con los registros de la Organización Mundial de la Salud (OMS) en este momento hay 34 vacunas candidatas a prueba en seres humanos y más de 100 en fase preclínica (aún en laboratorio antes de ser probadas en personas).
De los que están en etapa clínica, nueve están en fase III (aunque una, la de la compañía Janssen, no ha comenzado a reclutar participantes).
Son varias las compañías e institutos de investigación en la búsqueda: Cansino Biologic, el Instituto de Biotecnología de Pekín, el Instituto de Investigación Gamaleya (Rusia), la farmacéutica Janssen, el laboratorio Sinovac, la empresa Moderna, el Instituto de Biología de Wuhan, Pfizer y Novavax, entre otros.
Costa Rica incluso comenzó negociaciones con tres farmacéuticas, entre ellas AstraZeneca, en busca de asegurar acceso a alguna de las dosis, cuanto estén listas.
