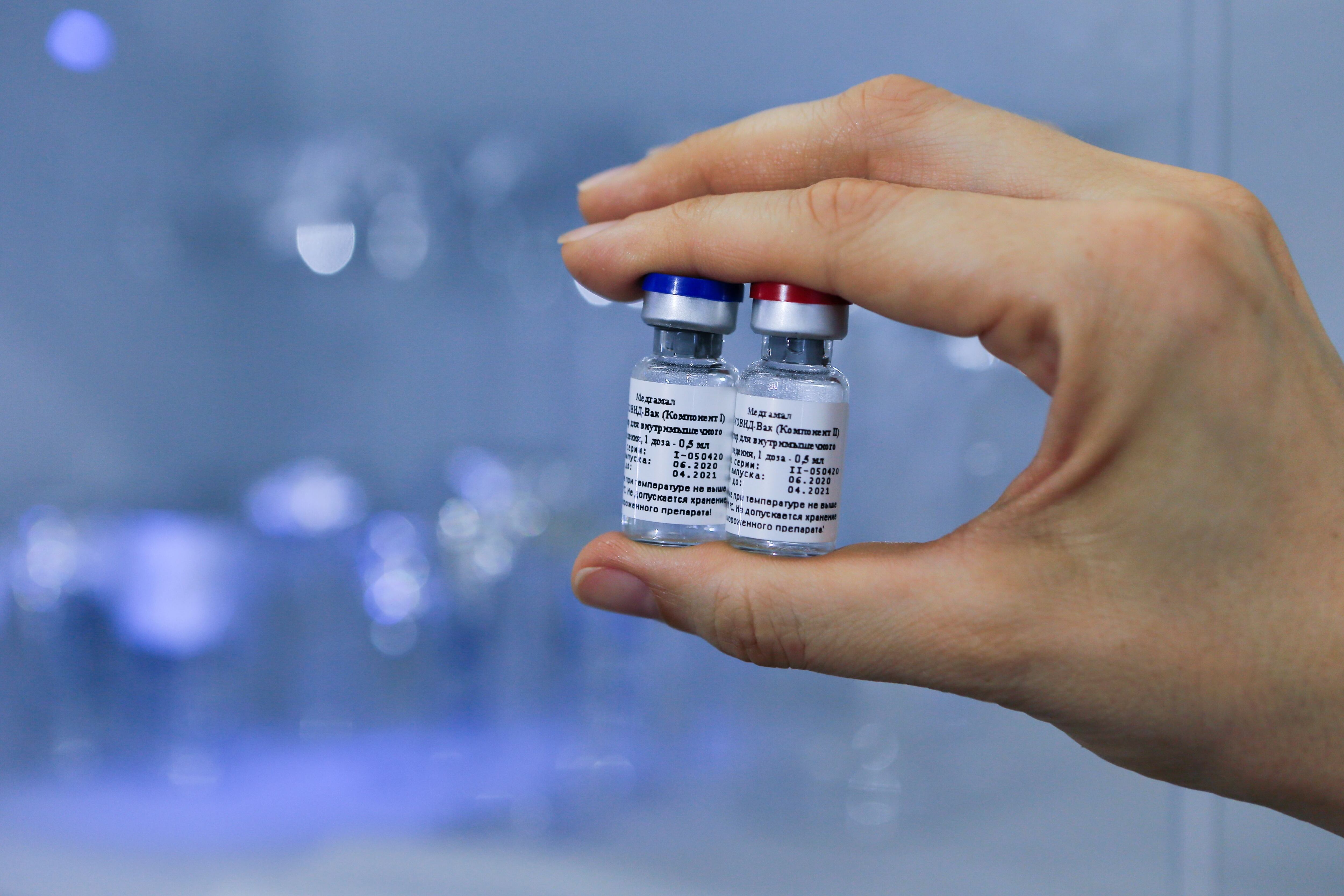
Este miércoles, el Instituto de Investigación en Epidemiología y Microbiología Gamaleya, en Rusia, salió a la prensa a decir que sus ensayos de fase III de la vacuna Sputnik V contra la covid-19 tienen una eficacia del 92%, dos puntos porcentuales por encima de los que la compañía farmacéutica Pfizer y la biontecnológica BioNTech anunciaron el lunes.
Según comentó Daniel Salas, ministro de Salud, en setiembre pasado, Costa Rica está en negociaciones para conseguir ambas vacunas. El presidente de la República, Carlos Alvarado, confirmó el lunes que el país negocia dosis para 1,5 millones de personas con Pfizer, pero no ha hablado del desarrollo ruso.
¿Los resultados anunciados quieren decir que la vacuna será aprobada pronto por entes reguladores internacionales y saldrá al mercado?
No. No es así de fácil, ni para estas dos ni para ninguna de las otras ocho que se encuentran en la fase III de ensayos en seres humanos. La tercera fase de pruebas es la última antes de su aprobación, pero también puede paralizarse o desecharse si no consigue los resultados esperados.
Es bueno tomar en cuenta que ambos anuncios son preliminares, es decir “a mitad de camino”, pues en los dos ensayos clínicos se encuentran en proceso y aún no se tienen resultados finales.
LEA MÁS: (Video) Maduro pronostica vacunación masiva contra covid-19 a partir de abril en Venezuela
Con reservas
Dentro de la comunidad científica hay muchas personas que, aun cuando ven estas noticias como buenas, no confían del todo.
¿Por qué? Ambas empresas hicieron sus anuncios a través de comunicados de prensa y publicaciones en sus redes sociales.
De momento, los resultados no han sido comunicados a la comunidad científica con la rigurosidad del caso.
Normalmente, los resultados de un ensayo clínico son sometidos a una revista científica. Antes de su publicación, el texto es sometido a un proceso de revisión por pares: un grupo de expertos en la materia para que garantizan veracidad, confiabilidad, integridad y consistencia de los datos. Ellos enviarán sus dudas y pedirán correcciones y, una vez que estas estén, se publica.
Sin embargo, aún ninguna de las dos vacunas experimentales han comunicado así sus resultados más recientes. Sí lo hicieron con sus resultados iniciales, que eran muy incipientes para hablar de eficacia.
Esta semana, el discurso cambió, pero todavía no hay publicaciones científicas. Ambas compañías anunciaron que estos resultados están prontos a publicarse, pero no dieron fechas.
Por ello, muchos científicos no se atreven a dar su opinión. Otros, optan por el llamado “optimismo cauto”: celebran el logro, pero con reservas.
“Esto es fantástico, sí debemos ver los resultados al final y ver si se mantienen, tenemos razones de estar optimistas... con los pies en la tierra”, dijo a la revista Nature Florian Krammer, virólogo de la Universidad Mount Sinai, en Estados Unidos.
La viróloga estadounidense Angela Rasmussen, dijo en su cuenta de Twitter: “mi sugerencia es estar felices de que los ensayos clínicos muestren resultados favorables, pero no tratar esto como si fuera información respaldable, no hasta que no tener más datos. Seamos pacientes”.
Tener los resultados en fase III no es el único paso. Después de eso, las compañías deben acudir a agencias reguladoras como la Agencia de Alimentos y Medicamentos de Estados Unidos (FDA, por sus siglas en inglés) o la Agencia Europea de Medicamentos (EMA) y esperar aprobación.
Pfizer y BioNTech adelantaron que pedirán una aprobación de emergencia ante la FDA (un aval temporal que se da cuando no hay vacunas para una condición considerada prioritaria) al finalizar noviembre.
Incluso con esta aprobación de emergencia, se debe seguir a los participantes del estudio durante meses para ver si se infectan o si tienen efectos adversos.
LEA MÁS: Mapa del coronavirus en Costa Rica: datos del Ministerio de Salud
LEA MÁS: UE prevé llegada de primeras vacunas contra covid-19 a inicios del 2021
Similitudes de ambas vacunas
Además de que buscan evitar la infección contra el virus SARS-CoV-2, causante de la covid-19, son pocas las semejanzas entre las opciones que dan el Instituto Gamaleya y la alianza de Pfizer y BioNTech.
Tal vez la principal similitud es que ambas están en la fase III de desarrollo de medicamento, en donde ya se analiza su eficacia (que funcione) y su seguridad (que sus efectos adversos sean menores a sus beneficios) en un mayor número de personas. De aprobarse, podrían comercializarse y utilizarse en los países donde así lo decidan las autoridades de salud.
Otra de las similitudes es que ambas son inyectadas y que consisten en dos dosis aplicadas con 21 días de diferencia.
LEA MÁS: Así se ve la curva de casos confirmados de covid-19 en Costa Rica
Las diferencias
Radican principalmente en la forma en la que buscan evitar la infección. Una de ellas, la de Pfizer y BioNTech, utiliza una técnica de ARN nunca antes utilizada en vacunas (pero sí a prueba en varias de las que se estudian hoy).
Mientras tanto, la vacuna rusa usa un método ya más conocido y que utiliza partes de otro virus para obtener una respuesta del cuerpo.
“Son dos caminos diferentes para llegar a un mismo objetivo y prevenir la infección con el virus”, manifestó Jarbas Barbosa, subdirector de la Organización Panamericana de la Salud (OPS).
La novedad, con condiciones de almacenamiento muy difíciles
La vacuna de Pfizer y BioNTech utiliza un tipo de tecnología que hasta el momento no se encuentra en ninguna vacuna aprobada: el ARN mensajero o ARNm.
Esta sustancia es parte de todas nuestras células. Su principal misión es transferir información a una parte de la célula llamada citoplasma para que, con base en estos datos, se generen proteínas.
Cuando un virus ingresa al cuerpo, lo engaña, pues actúa como ARNm y pone al citoplasma a trabajar para él y crear las proteínas necesarias para que el virus se replique.
Con una vacuna, esta pondría al cuerpo a trabajar contra el virus.
Los científicos copian la información del virus y ese pedacito genético, su ARNm, se pone en la vacuna y codifica un antígeno (tipo de proteína) específico de la enfermedad. Una vez que la cadena de ARNm está dentro de las células, estas usan la información genética para producir el antígeno.
No obstante, para que las características del ARNm se preserven este debe estar a -70° C, lo que requiere sistemas de congelación específicos con los que aún no se cuentan.
La buena noticia es que este producto puede subir a un máximo de 5° C cinco días antes de su aplicación, por lo que sí podría estar en refrigeración en los centros de salud.
LEA MÁS: Especial: La covid-19 en Costa Rica
La carrera por una vacuna
FUENTE: OMS, PFIZER, SANOFI-PASTEUR, CDC, FDA, CLINICALTRIALS.GOV || w.s. / LA NACIÓN.
LEA MÁS: Cantones con coronavirus en Costa Rica: Datos del Ministerio de Salud
La apuesta rusa: adaptación de un camino más conocido
Mientras tanto, la vacuna de Gamaleya utiliza un vector viral para su cometido. En otras palabras, se utiliza un virus ya conocido como “vehículo”; se le diseña genéticamente para que pueda producir proteínas de coronavirus en el cuerpo.
Estos virus están debilitados para que no puedan causar enfermedades.
Esta vacuna experimental usa un tipo de virus denominado adenovirus. Se trabaja específicamente con uno llamado Ad5 (adenovirus 5) para la primera inyección y el Ad26 (adenovirus 26) para la segunda.
Pero, a diferencia de otras vacunas que utilizan adenovirus, en esta los virus no se pueden replicar dentro de la célula. Es una vacuna de tipo “no replicante” en la que los vectores virales no son capaces de multiplicarse o crear copias de sí mismos.
La vacuna de la Universidad de Oxford y la farmacéutica AstraZeneca también funciona bajo el mismo esquema, con la diferencia de que ellos utilizan una adenovirus que afecta a chimpancés y no a seres humanos.
Dentro de sus ventajas está el que no requiere mantenerse a niveles altos de congelación y bajas temperaturas. En este caso, solo es necesario estar entre 2 ° C y 8 ° C, como la gran mayoría de vacunas que se tienen en Costa Rica. Con esto, se haría más fácil su administración.
LEA MÁS: 3.000 ticos participarán en estudio sobre inmunidad contra covid-19